製造販售有效成分為zolpidem tartrate之安眠藥IntermezzoR的美國藥廠Purdue Pharmaceutical L.P與Purdue Pharma L.P. (下稱Purdue),以及研發IntermezzoR的藥物研發公司Transcept Pharmaceutical, Inc. (下稱Transcept,其為本案系爭專利之專利權人,而Purdue則為系爭專利的專屬被授權人),以共同原告身分在2013年8月20日與8月22日,分別向美國紐澤西州聯邦地院與伊利諾州北區聯邦地院提起兩起專利侵權告訴(兩案訴狀內容幾近一致),控告我國致力於開發學名藥、亦投入創新醫藥品研發的安成國際藥業股份有限公司(TWi Pharmaceuticals, Inc.,下稱安成藥業),其向美國食品藥物管理局(FDA)提出申請IntermezzoR之學名藥上市許可的行動(ANDA No. 205061),就本案2項系爭專利構成侵權行為。
本案兩項系爭專利之內容如下:
- 美國專利編號US 8,252,809,名稱為「治療失眠之成分(Compositions for treating insomnia)」,於2012年8月28日核發,發明人為Transcept的資深副總裁與首席研發長Nikhilesh Singh;
- 美國專利編號US 8,242,131,名稱為「治療午夜失眠之方法(Methods of treating middle-of-the-night insomnia)」,於2012年8月14日核發,共同發明人為Nikhilesh Singh以及Sathasivan Indiran Pather。
在美國要生產販售特定品牌藥之學名藥,須向FDA提出「簡易新藥申請」(Abbreviated New Drug Application, ANDA)無須像「新藥申請」(New Drug Application, NDA)一樣提供藥物安全性與有效性之資料,而可以援用FDA核准品牌藥上市時就其安全性與有效性所得出的結論。而面對學名藥產品可能侵害品牌藥專利權利的爭端,法規一方面要求品牌藥廠須在所謂「橘皮書」(the Orange Book)中列出相關專利的證號與有效日期,另一方面要求學名藥廠在其ANDA中保證其學名藥不會侵害品牌藥廠的專利權利。
對前述法規要求,學名藥廠可以舉證品牌藥廠未列出任何專利或專利已過期、或要求上市許可之起始日在專利到期後、或舉證專利無效或其學名藥產品未構成侵權;最後一種方式被稱為paragraph IV certification,在美國專利法上會被視為專利侵權行為而專利權人(品牌藥廠)可據以起訴,而品牌藥廠若在45天內起訴,FDA必須以30個月為期中止審查程序,在中止期間若法院做出專利有效性或侵權認定之判決,則FDA依據判決結果來處理,若期間法院未做出判斷,則30個月後FDA將繼續進行程序。
基於上述規定,安成藥業在其興櫃公告中對此事件之說明為「此專利侵權訴訟係法規程序,因產品尚未上市,故無侵權賠償問題」。而本案原告則是在其訴狀中請求法院認定侵權行為成立、核發命令要求FDA所核發上市許可、不得早於系爭專利到期日、以及對任何侵害系爭專利權利之產品(包括本案系爭學名藥產品)核發禁制令等。
另外,安成藥業在2013年7月31日時亦公告,其與生產Amrix藥品的以色列藥廠Teva Pharmaceutical Industries, Ltd.達成和解協議,Teva將撤銷在美國對其所提出Amrix藥品的專利侵權訴訟並授權本公司生產的學名藥產品於專利到期前於美國銷售。而根據報導指出,安成藥業共9項藥品採取paragraph IV certification之方式申請美國FDA核准中,其中7項已在2011年提出學名藥上市申請,預期2013年下半年可望有2到3項產品上市。(1483字;表2)
表一、請求項解析
| US 8,242,131 請求項1 |
US 8,252,809 請求項1 |
1. A method of treating middle-of-the-night insomnia in a non-elderly patient without prophylactically administering zolpidem, comprising:
一項不進行zolpidem預防性投藥而用來治療非年長患者午夜失眠症狀的方法,包括 |
1. A solid unit dosage composition for the treatment of MOTN insomnia,
一項用來治療午夜失眠的固態藥劑成分 |
dosing the patient with a pharmaceutical composition comprising about 0.5 to about 4.75 mg of zolpidem hemitartrate or a molar equivalent amount of a pharmaceutically acceptable form of zolpidem,
提供病患服用,以約0.5至4.5毫克zolpidem hemitartrate所構成之醫藥成分,或質量相等、藥學上可接受型態的zolpidem |
said composition comprising an effective amount of zolpidem or a salt thereof, formulated for delivery of zolpidem across a subject's oral mucosa,
前述成分是由有效劑量之zolpidem或含有zolpidem之鹽化合物所構成,其劑型讓zolpidem可以通過服用者口腔黏膜來制放 |
wherein the pharmaceutical composition is substantially free of other hypnotic agents, wherein the patient awakens from sleep, and desires to resume sleep for less than 5 hours, wherein the step of dosing the pharmaceutical composition is performed after the patient awakens from sleep, and wherein the pharmaceutical composition permits the patient to awaken at a time about four hours after dosing without residual sedative effects.
前述醫藥成分並未含其他安眠劑,前述病患是從睡眠中醒來並希望恢復少於5小時的睡眠,服用前述醫藥成分之步驟是在前述病患從睡眠中醒來後進行,而前述醫藥成分讓前述病患在約4小時的時間後醒來且不會有殘餘中樞抑制的效果 |
wherein said effective amount is an amount of less than 1.30×10-5 moles of zolpidem, and is an amount sufficient to produce a plasma concentration between about 25 ng/ml and about 50 ng/ml within 20 minutes of administration, when evaluated in an appropriate patient population.
前述有效劑量是少於1.30×10-5莫耳之zolpidem的量,且為以適當病患族群來測試可以在投藥20分鐘內產生約25 ng/ml至50 ng/ml之血液濃度之劑量 |
FIG. 3 shows the Digit Symbol Substitution Test (DSST) scores of a 1.0 mg, 1.75 mg, and 3.5 mg sublingual zolpidem lozenge of the present invention as a function of time.
FIG.3表示服用1.0毫克、1.75毫克與3.5毫克之本發明的舌下含服zolpidem含片後,進行數字符號代換測驗(DSST)之分數結果,其顯示本發明之時間作用
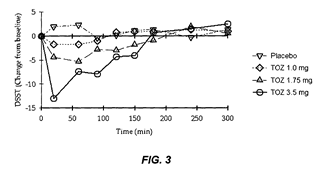 |
FIG. 1 shows the mean (SEM) plasma concentration time profiles of a 1.0 mg, 1.75 mg, and 3.5 mg sublingual zolpidem lozenge of the present invention.
FIG.1表示1.0毫克、1.75毫克與3.5毫克之本發明的舌下含服zolpidem含片,其隨時間產生之平均血液濃度
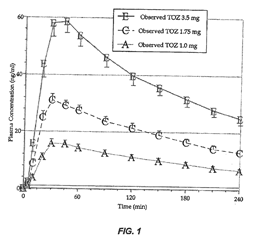 |
Source: 科技政策研究與資訊中心—科技產業資訊室整理,2013/08
表二、專利訴訟案件基本資料
Puedue控告安成藥業之學名藥侵害其專利權利
| 訴訟名稱 |
Purdue Pharmaceutical Products LP et al v. TWi Pharmaceuticals Inc. |
Purdue Pharmaceutical Products LP et al v. TWi Pharmaceuticals Inc. |
| 提告日期 |
2013年8月20日 |
2013年8月22日 |
| 原告 |
Purdue Pharmaceutical Products LP
Purdue Pharma LP
Transcept Pharmaceuticals Inc. |
Purdue Pharmaceutical Products LP
Purdue Pharma LP
Transcept Pharmaceuticals Inc. |
| 被告 |
TWi Pharmaceuticals Inc. |
TWi Pharmaceuticals Inc. |
| 案號 |
2:13-cv-05003-JLL-JAD |
1:13-cv-05999 |
| 訴訟法院 |
the U.S. District Court for the District of New Jersey |
the U.S. District Court for the Northern District of Illinois |
| 系爭專利 |
US 8,242,131
US 8,252,809 |
US 8,242,131
US 8,252,809 |
| 系爭產品 |
安成藥業的學名藥尚未被核准上市,而Purdue所生產的品牌藥IntermezzoR,其相關資訊可見:http://www.intermezzorx.com/ (最後瀏覽日:2013/08/30) |
安成藥業的學名藥尚未被核准上市,而Purdue所生產的品牌藥IntermezzoR,其相關資訊可見:http://www.intermezzorx.com/ (最後瀏覽日:2013/08/30) |
| 訴狀下載 |
 |
 |
Source: 科技政策研究與資訊中心—科技產業資訊室整理,2013/08
--------------------------------------------------------------------------------------------------------------------------------------------